Laboratorní příručka
| Karbonylhemoglobin_Ba |
| Jednotky: | 1 |
| Princip stanovení: | oxymetrie |
| Odběr: |
| Odebíraný vzorek: | Krev arteriální |
| Doporučený odběr do: | ABR - Plast, Ca balanc. heparin (Sarstedt, Radiometer) |
| Stabilta vzorků: |
| Stabilita při 20 - 25 °C : | 15 min |
| Stabilita při 2 - 8 °C: | 1 h |
| Provádíme: |
| Příjem vzorků pro rutinu: | Denně |
| Příjem vzorků pro statim: | Denně, 24 hodin |
| Odezva na statim: | Do 15 min.od doručení |
| Vyšetření provádí: | Úsek vnitřního prostředí OKB |
| Referenční a interpretační meze: |
| Věk od | do | Dolní ref. mez | Horní ref. mez | Jednotka | Další údaje | |
| 0D | 99R+ | 0,00 | 0,015 | 1 |
| Zdroj referenčních hodnot: | Příbalový leták |
| Pokyny k odběru: |
|
Odběr arteriální krve provést anaerobně do odběrové zkumavky s Ca balancovaným heparinem (ABR). Odebraná krev nesmí
obsahovat vzduchové bubliny, proto je nutné ihned po odběru je ze stříkačky vytlačit. Krev v odběrové zkumavce je nutné
po odběru řádně ale opatrně promíchat a ihned poslat do laboratoře. |
| Pokyny k preanalytice: |
| Zpracovat do 15 minut po odběru. |
| Klinické informace : |
|
Charakteristika Acidobazická rovnováha je spojena s metabolismem vodíkových iontů (H+), tedy s oxidoredukčními pochody provázejícími buněčný metabolismus. Koncentrace (přesněji aktivita) vodíkových iontů c[H+], respektive protonový gradient na intra- i extracelulárních membránách ovlivňuje buněčný metabolismus. Proto udržování aktivity H+ v určitých mezích je životně důležité. Změnou c[H+] se mění biologická aktivita proteinů, distribuce a stupeň ionizace elektrolytů apod. Pro organismus je proto velmi důležité udržovat koncentraci (aktivitu) vodíkových iontů v určitých mezích, i když tato koncentrace se pohybuje o 3–4 řády níže než koncentrace jiných iontů. V extracelulární tekutině se udržuje c[H+] kolem hodnoty 40 mmol/L, zatímco c[Na+] činí průměrně 145 mmol/L. V různých buněčných kompartmentech je však koncentrace H+ různá, vyjádříme-li ji jako hodnotu pH, pak v cytosolu buněk se udává pH 6,700–7,200; v některých organelách jako jsou lysozomy, Golgiho aparát pod 5,000; v jiných (mitochondrie) naopak vyšší než 7,400.
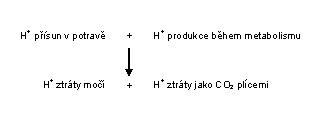
Poruchy acidobazické rovnováhy vznikají, jestliže následující rovnice nejsou vyváženy:
Hodnota kyseliny uhličité (vyjádřená jako pCO2) se mění při poruchách, které označujeme jako respirační. Hodnota hydrogenuhličitanu se mění při poruchách, které označujeme jako metabolické. Podstatou života z biochemického hlediska jsou metabolické děje, jejichž cílem je zisk energie a substrátů potřebných pro enzymatické reakce. Jde převážně o aerobní procesy, při nichž se rozpadají složité sloučeniny uhlíku a vodíku a vznikají jednodušší látky, většinou kyselé povahy. Denně se tímto způsobem vytvoří asi 20 000 mmol oxidu uhličitého a 70 mmol netěkavých kyselin, převážně fosfátů a sulfátů. Nekontrolované hromadění těchto látek v organismu by znamenalo pokles pH extracelulární tekutiny a ve svých důsledcích narušení až znemožnění životních dějů. Výchylkám pH krve mimo referenční interval, ať už ve smyslu acidémie (poklesu pod dolní hranici referenčního rozmezí) nebo alkalémie (vzestupu nad horní hranici referenčního rozmezí), je organismus schopen čelit několika způsoby: pomocí pufrovacích systémů krve a činností plic, ledvin nebo dalších orgánů. Poruchy acidobazické rovnováhy se mohou vzájemně kombinovat nebo kompenzovat. Souvisí také s iontovou nerovnováhou vnitřního prostředí a jsou výsledkem četných primárních klinických chorob spojených s poruchami látkového metabolismu.
Měření ABR Měření se provádí na speciálních acidobazických analyzátorech, které současně měří řadu parametrů obvykle v kapiláře v průtokovém režimu (pH, pCO2 pO2, Na+, K+,Cl- Ca+2 ev. další parametry). Tyto přístroje pak dopočítají další parametry nutné pro hodnocení. Analyzátor ABL 835 FLEX měří na principu potenciometrie (pH, pCO2, ionty) a ampérometrie (pO2, glukóza, laktát) a spektrofotometrie (hemoglobin a jeho frakce, bilirubin).
Měřené parametry: pH, pCO2, pO2, Na+, K+, Cl-, iCa2+, Lac, Glu, tHb, FO2Hb, FCOHb, FMetHb, FHHb, FHbF, celkový bilirubin, aktuální HCO3-
Vypočtené parametry: SO2, standardní HCO3- (pCO2 5,3 kPa), BE (base excess), iCa2+ korigované (pH 7,4), SID (diference silných iontů), AG (anion gap)…
Výpovědní hodnota SO2 Okysličení tkání závisí na vychytávání kyslíku v plicích (oxygen uptake), podmínkách jeho transportu krví (oxygen transport) a na dostatečném uvolňování kyslíku do tkání (oxygen release). Mezi ukazatele transportu kyslíku krví patří hodnoty hemoglobinu a jeho derivátů (metHb, COHb, sulfHb) a saturace hemoglobinu kyslíkem.
Přenos kyslíku krví je umožněn vazbou na protein tetramerní struktury – hemoglobin. Hemoglobin A je tvořen čtyřmi podjednotkami (2α, 2β). Každá z podjednotek má globinovou a hemovou část. Hem je planární tetrapyrolový kruh s centrálně uloženým atomem Fe2+. Atom železa má šest koordinačních vazeb (čtyři valence směřují k dusíkům čtyř pyrolových jader, pátá vazba poutá histidin globinu a šestá valence je volná pro kyslík). Vazbou kyslíku na železo hemu vzniká oxyhemoglobin.
Každý gram hemoglobinu je schopen vázat a přenášet 1,34 ml kyslíku. Vazba kyslíku na hemoglobin však neprobíhá rovnoměrně – zpočátku je obtížná a energeticky málo výhodná, protože je při ní nutné zrušit většinu elektrostatických vazeb mezi podjednotkami α a β. Snazší navazování dalších molekul kyslíku je vyjádřeno tvarem (strmostí) disociační křivky hemoglobinu (závislost nasycení hemoglobinu na parciálním tlaku kyslíku).
Potenciální kapacita krve pro transport kyslíku je vyjádřena koncentrací celkového hemoglobinu. Část hemoglobinu je vlivem různých škodlivin (dusitany, dokonce i některé léky) oxidována na methemoglobin (hemiglobin) s trojmocným železem, který není schopen vázat kyslík, nebo vzniká karbonylhemoglobin (COHb) při otravách oxidem uhelnatým a sulfhemoglobin (SulfHb) při otravě sirovodíkem. Tyto formy hemoglobinu jsou překážkou fyziologickému transportu kyslíku krví. Saturace hemoglobinu kyslíkem dává spolu s celkovou koncentrací hemoglobinu a parciálním tlakem kyslíku informaci o schopnosti krve transportovat kyslík tkáním.
Kyslíkové parametry a hemoglobin Metabolismus kyslíku je neoddělitelně spjat s acidobazickým metabolismem a sleduje se současně s ABR. Pro správnou terapii pacientů na řízeném dýchání je nutný hlubší obraz metabolismu O2 („Deep picture“) V klinické praxi jsou kromě základní hodnoty pO2 požadovány další, změřené a vypočtené parametry:
Saturace Hb (SO2) Parametr SO2 informuje o efektivitě oxygenační terapie. Součet cHHb+cO2Hb představuje efektivní hemoglobin (ceHb). Výpočet saturace je potom SO2 = cO2Hb/ceHb.
Kyslíkový parametr p50 (kPa) je tlak kyslíku v krvi, při kterém je hodnota saturace hemoglobinu 50%. Jeho výpočet se provádí automaticky po změření venosní krve. Charakterizuje umístění disociační křivky hemoglobinu, je ukazatelem afinity hemoglobinu ke kyslíku a je kritériem pro uvolňování kyslíku z HbO2 do tkání. Vysoké hodnoty p50 v případě posunu křivky doprava (snížená afinita Hb ke kyslíku, tj. snadné uvolňování O2), se vyskytují např. u anemie, kde je uvolňování kyslíku v tkáních usnadněno.
Methemoglobin (MetHb) je derivát hemoglobinu, kde je železo v trojmocné formě, bylo tedy oxidováno na Fe3+ a v takové formě není schopno vázat kyslík. Vysoká koncentrace methemoglobinu v krvi (methemoglobinemie) může být příčinou hypoxie a cyanosy. Methemoglobinemii vyvolávají toxické látky, jako jsou nitráty, nitrity, anilinové sloučeniny, různá anestetika (benzokain). Novorozenci vykazují zvýšenou tvorbu methemoglobinu vzhledem k tomu, že fetální hemoglobin (HbF) se snadněji oxiduje na MetHb než hemoglobin dospělých (HbA). Karbonylhemoglobin (COHb) je derivát hemoglobinu, kde je kovalentně (pevně) vázán oxid uhelnatý (CO) na Fe2+. Afinita hemoglobinu je k CO 280x vyšší než k O2. COHb není vzhledem k pevnosti vazby CO schopen přenášet kyslík a jeho vysoké hodnoty při intoxikacích jsou také příčinou hypoxie a cyanózy, někdy s fatálními důsledky. Mírné intoxikace CO jsou léčeny v kyslíkových hyperbarických komorách.
Výpovědní hodnota karbonylhemoglobin Karbonylhemoglobin (karboxyhemoglobin) patří mezi dyshemoglobiny (spolu s methemoglobinem a sulfhemoglobinem), kdy je vazebné místo pro kyslík (tj. dvojmocné železo) obsazeno oxidem uhelnatým. Hemoglobin má 200 až 280x větší afinitu pro oxid uhelnatý než pro kyslík, se stoupajícím podílem karbonylhemoglobinu v krvi klesá schopnost hemoglobinu vázat kyslík. Vzniká intoxikací, terapie založena na zvýšení podílu kyslíku rozpuštěného v plazmě. Výrazné riziko hypoxie se proto týká zejména anemických pacientů. Disociační křivka kyslíku je posunuta doleva, takže vázne uvolňování kyslíku do tkáně. Se stoupající fyzickou aktivitou stoupá vazba oxidu uhelnatého na hemoglobin. Fetální karbonylhemoglobin dosahuje koncentrací o 10 až 15 % větší než odpovídající koncentrace karbonylhemoglobinu u matky. Za normálních okolností je v krvi přítomno malé množství karbonylhemoglobinu. Část je způsobena endogenním vznikem při myolýze a hemolýze (z tohoto důvodu je při neonatální hyperbilirubinemii až 0,12, tj. 12 % karbonylhemoglobinu). U normálních kuřáků tabáku je podíl karbonylhemoglobinu na celkovém hemoglobinu v krvi 0,02 - 0,10 (tj. 2-10, výjimečně i 15 %) karbonylhemoglobinu.
Stav se zvýšením karbonylhemoglobinu je nazývá karbonylhemoglobinémie (karboxyhemoglobinémie). Posun disociační křivky doleva (zhoršení uvolňování kyslíku). Léčba zabráněním další intoxikace, adekvátní ventilací s udržováním vysokého pO2 nebo hyperbarická léčba. Cílem terapie je zvýšit celkovou koncentraci kyslíku (ctO2) ve složce rozpuštěného O2, protože je sice vysoká funkční saturace (sO2), ale současně při při přítomnosti dyshemoglobinu (COHb) snížen podíl efektivního hemoglobinu.
Cílem terapie je tedy zvýšit hodnotu druhého sčítance v rovnici:
ctO2 = sO2 * (1-COHb – MetHb) + α * pO2
kde α je koeficient solubility kyslíku v plazmě.
Nejčastěji toxická karbonylhemoglobinémie při průmyslových otravách, při požárech, z výfukových plynů (suicidia). Mírná subintoxikace u silných kuřáků. Přechodem na zemní plyn vymizely sebevraždy svítiplynem.
Třešňově zbarvená krev.
Do podílu karbonylhemoglobinu na celkovém hemoglobinu v krvi 0,15 až 0,20 (tj. 15 až 20 %) nejsou symptomy, mezi 10 až 20 % se však může objevit bolest hlavy. Do 0,50 (tj. 50 %) karbonylhemoglobinu je nauzea, slabost, obtížné dýchání, bezvědomí nastává mezi 0,50 - 0,70 (tj. 50–70 %) karbonylhemoglobinu. Život ohrožuje koncentrace nad 0,80 (tj. 80 %) karbonylhemoglobinu, kdy může nastat náhlé úmrtí. Letální však mohou být podíly nad 0,50 (tj. 50 %). Rychlá smrt nad 0,80 (tj. 80 %) a fatální případy obvykle nad 0,60 (tj. 60 %).
Poločas karbonylhemoglobinu u osob s normální funkcí kardiopulmonálního aparátu je 1 až 2 hodiny.
Zdroje Masopust, J.: Klinická biochemie I. a II., Praha 1998, Racek, J. a spol.: Klinická biochemie, Praha 1999, Zima, T.: Laboratorní diagnostika, 2.vydání, Praha, Galén 2007, Schneiderka,Petr, et al.: Kapitoly z klinické biochemie. 2. vyd.,Praha, Karolinum 2004, VEJRAŽKA, Martin. Poruchy acidobazické rovnováhy [přednáška k předmětu Patobiochemie, obor Všeobecné lékařství, 1. LF UK]. Praha. 7.12.2010.
|

 Cookies
Cookies